სინოფარმი (პეკინი): BBIBP-CorV
ფაზა 1
1 სასამართლო
ChiCTR2000032459
ჩინეთი
ფაზა 2
2 ცდა
NCT04962906
არგენტინა
ChiCTR2000032459
ჩინეთი
ფაზა 3
6 ცდა
NCT04984408
ChiCTR2000034780
არაბთა გაერთიანებული საამიროები
NCT04612972
პერუ
NCT04510207
ბაჰრეინი, ეგვიპტე, იორდანია, არაბთა გაერთიანებული საამიროები
NCT04560881, BIBP2020003AR
არგენტინა
NCT04917523
არაბთა გაერთიანებული საამიროები
დამტკიცებები
WHO საგანგებო გამოყენების ჩამონათვალი 59 ქვეყანა
ანგოლა 、 არგენტინა 、 ბაჰრეინი 、 ბანგლადეში 、 ბელორუსია 、 ბელიზი 、 ბოლივია (Plurinational State of) 、 ბრაზილია 、 ბრუნეის დარუსალამი 、 კამბოჯა 、 კამერუნი 、 ჩადი 、 ჩინეთი 、 კომორის კუნძულები 、 ეგვიპტე 、 ეკვატორული გვინეა 、 გაბონი 、 გამბია 、 საქართველო 、 გვიანა 、 საქართველო 、 ირანი (ისლამური რესპუბლიკა) 、 ერაყი 、 იორდანია 、 ყირგიზეთი 、 ლაოსის სახალხო დემოკრატიული რესპუბლიკა
ლიბანი 、 მალაიზია 、 მალდივები 、 მავრიტანია ur აურიტიუსი 、 მონღოლეთი 、 ჩერნოგორია 、 მაროკო 、 მოზამბიკი 、 ნამიბია 、 ნეპალი 、 ნიგერი 、 ჩრდილოეთ მაკედონია 、 პაკისტანი 、 პარაგვაი 、 პერუ 、 ფილიპინები Cong კონგოს რესპუბლიკა 、 ენერგელეს 、 სერბია 、 სერგეალი 、 სერბეთი კუნძულები 、 სომალი 、 შრი ლანკა 、 ტაილანდი 、 ტრინიდადი და ტობაგო 、 ტუნისი Arab არაბთა გაერთიანებული საამიროები 、 ვენესუელა (ბოლივარიის რესპუბლიკა) 、 ვიეტნამი 、 ზიმბაბვე
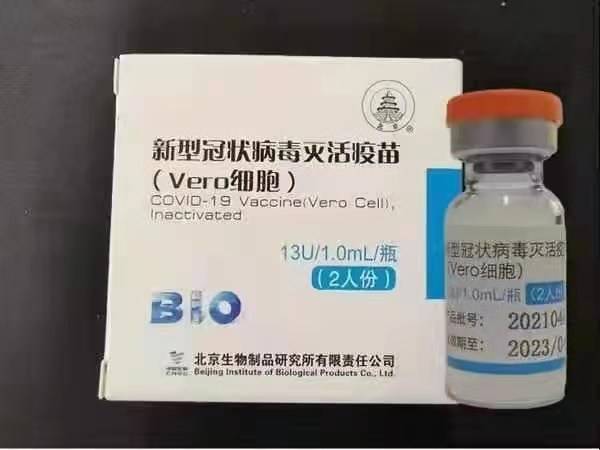
Sinopharm BBIBP-CorV COVID-19 არის ინაქტივირებული ვაქცინა, რომელიც დამზადებულია კულტურულად გაზრდილი ვირუსის ნაწილაკებისგან, რომლებსაც არ გააჩნიათ პათოგენური უნარი. ეს ვაქცინის კანდიდატი შემუშავებულია Sinopharm Holdings– ისა და პეკინის ბიოლოგიური პროდუქტების ინსტიტუტის მიერ.
Sinopharm BBIBP-CorV ვაქცინა მუშაობს იმუნური სისტემის საშუალებით, რომელიც აწარმოებს ანტისხეულებს SARS-CoV-2 ბეტა კორონავირუსის წინააღმდეგ. ათწლეულების განმავლობაში გამოიყენება ინაქტივირებული ვირუსული ვაქცინები, როგორიცაა ცოფის ვაქცინა და A ჰეპატიტის ვაქცინა. განვითარების ეს ტექნოლოგია წარმატებით იქნა გამოყენებული ბევრ ცნობილ ვაქცინზე, როგორიცაა ცოფის ვაქცინა.
სინოფარმის SARS-CoV-2 შტამი (WIV04 შტამი და ბიბლიოთეკის ნომერი MN996528) იზოლირებული იყო პაციენტისგან ჩინეთში, ვუჰანში, ჯინიინტანის საავადმყოფოში. ვირუსი გავრცელდა კულტურაში კომპეტენტურ ვერო უჯრედულ ხაზში, ხოლო ინფიცირებული უჯრედების სუპერნატანი ინაქტივირებულია β- პროპიოლაქტონთან (1: 4000 ვოლტ/მოცულობა, 2-დან 8 ° C) 48 საათის განმავლობაში. უჯრედების ნამსხვრევების და ულტრაფილტრაციის დაზუსტების შემდეგ, მეორე β- პროპიოლაქტონის ინაქტივაცია განხორციელდა იმავე პირობებში, როგორც პირველი ინაქტივაცია. ჯანმო-ს თანახმად, ვაქცინა შეიწოვება 0.5 მგ ალუმზე და იტვირთება წინასწარ შევსებულ შპრიცებში 0.5 მლ ფოსფატის ბუფერული სტერილური მარილით, კონსერვანტების გარეშე.
2020 წლის 31 დეკემბერს, წამლის სახელმწიფო ადმინისტრაციამ გამოაცხადა სინოფარმის მიერ შემუშავებული ექსპერიმენტული ვაქცინის დამტკიცება.
2021 წლის 7 მაისს ჯანდაცვის მსოფლიო ორგანიზაციამ გამოაცხადა ვაქცინის დამტკიცების შესახებ. ჯანმო-ს საგანგებო გამოყენების ჩამონათვალმა ქვეყნებს საშუალება მისცა დააჩქარონ საკუთარი მარეგულირებელი ნებართვები COVID-19 ვაქცინის იმპორტისა და ადმინისტრირებისათვის. ჯანმო -ს იმუნიზაციის სტრატეგიების მრჩეველთა ექსპერტთა ჯგუფმა ასევე დაასრულა ვაქცინის მიმოხილვა. ყველა არსებული მტკიცებულების საფუძველზე, ჯანმო გვირჩევს ვაქცინის ორ დოზას, სამიდან ოთხ კვირაში ერთხელ, 18 წლის და უფროსებისთვის. ვაქცინის ეფექტურობა სიმპტომური და ჰოსპიტალიზირებული დაავადების წინააღმდეგ შეფასებულია 79% ყველა ასაკობრივი ჯგუფისათვის ერთად.
ამერიკის სამედიცინო ასოციაციამ გამოაქვეყნა "რანდომიზებული კლინიკური ცდა: 2 ინაქტივირებული SARS-CoV-2 ვაქცინის გავლენა მოზრდილებში COVID-19 სიმპტომურ ინფექციაზე" 2021 წლის 26 მაისს და დაასკვნა, რომ "რანდომიზებული კლინიკური კვლევის ამ წინასწარ განსაზღვრულ შუალედში, მოზრდილები 2 ინაქტივირებული SARS-CoV-2 ვაქცინა, რომელიც გამოიყენება რანდომიზებული კლინიკური კვლევების ამ წინასწარ განსაზღვრულ შუალედურ ანალიზში, მნიშვნელოვნად ამცირებს სიმპტომური COVID-19- ის რისკს და სერიოზული გვერდითი მოვლენები იშვიათი იყო. " ამ ფაზის 3 რანდომიზებული კვლევა მოზრდილებში, 2 ინაქტივირებული მთლიანი ვირუსის ვაქცინის ეფექტურობა COVID-19 სიმპტომურ შემთხვევებში იყო 72.8% და 78.1%, შესაბამისად. 2 ვაქცინას ჰქონდა იშვიათი სერიოზული გვერდითი მოვლენები მსგავსი სიხშირით მხოლოდ ალუმ-საკონტროლო ჯგუფის მიმართ და უმეტესობა არ იყო დაკავშირებული ვაქცინაციასთან. საძიებო ანალიზმა აჩვენა, რომ 2 ვაქცინამ გამოიწვია გაზომვადი ნეიტრალიზების ანტისხეულები, მსგავსია 1/2 ფაზის ცდის შედეგებისა.
WHO SAGE სამუშაო ჯგუფმა გამოაქვეყნა Sinopharm/BBIBP COVID-19 ვაქცინის მიმოხილვა 2021 წლის 10 მაისს. GAVI– ს COVID-19 ვაქცინა აერთიანებს ვაქცინის ფლაკონის მონიტორს, რომელიც ეუბნება ჯანდაცვის მუშაკებს, არის თუ არა ვაქცინა შენახული სწორად და არ არის გამოვლენილი გადახურება შედეგად, დაზიანება, GAVI იტყობინება 2021 წლის 14 მაისს. Zebra Technologies– ის მიერ დამზადებული ჭკვიანი ეტიკეტები და დამზადებულია Temptime Corporation– ისგან, შედგება წრისგან, რომლის შუაში არის ღია ფერის კვადრატი, დამზადებულია უფერო ქიმიკატისგან, რომელიც შეუქცევადად ავითარებს ფერს დროთა განმავლობაში რა ეს ხდება უფრო ბნელი, რომ ვიზუალური მითითება მოგვცეს კუმულატიური სითბოს ექსპოზიციის შესახებ. მას შემდეგ, რაც ფლაკონი ცხელდება მისი ოპტიმალური შენახვის დიაპაზონის მიღმა, კვადრატი უფრო მუქი ხდება ვიდრე წრე, რაც მიუთითებს იმაზე, რომ ვაქცინა აღარ უნდა იქნას გამოყენებული.
ეროვნული წამალი BBIBP-CorV COVID-19 ვაქცინის ნარკოტიკების ბიბლიოთეკის რეგისტრაციის ნომერი: DB15807.